«Es una observación clínica común que algunos pacientes sanos con hipotiroidismo continúen quejándose de fatiga, mal humor, incapacidad para concentrarse y dificultades cognitivas vagas (a menudo descritas), como «niebla mental») a pesar de los niveles normales de TSH » [PMCID: PMC5036318]. Ante esta observación nos parece interesante el enfoque de Moncayo y Moncayo para abordar el estudio de la función tiroidea, que relatamos a continuación. (PMID: 28417080),
Muchos pacientes no estaban contentos con su tratamiento ya sea por hipo o por hipertiroidismo. Algunos pacientes que habían tenido una tiroidectomía total aún hablaban de que la tiroides es responsable de su condición. El síntoma más común que hemos observado fue fatiga. Los siguientes síntomas más comunes fueron agotamiento, calambres musculares, dolores musculares, ritmo cardíaco irregular, nerviosismo, sudoración, irritabilidad, estado de ánimo depresivo, concentración deficiente y mala memoria, sensación de vértigo y cefalea. Este complejo cuadro clínico podría malinterpretarse como una enfermedad psicosomática. Al profundizar en esta situación clínica, pudimos identificar un denominador común detrás del «así llamado» complejo de síntomas de la enfermedad tiroidea, a saber, la deficiencia de magnesio (doi.org/10.1016/j.woman.2014.02.001 ).; por ello es necesario conocer el estado de los minerales en nuestro cuerpo para un correcto tratamiento de la enfermedad tiroidea y asi tenemos:
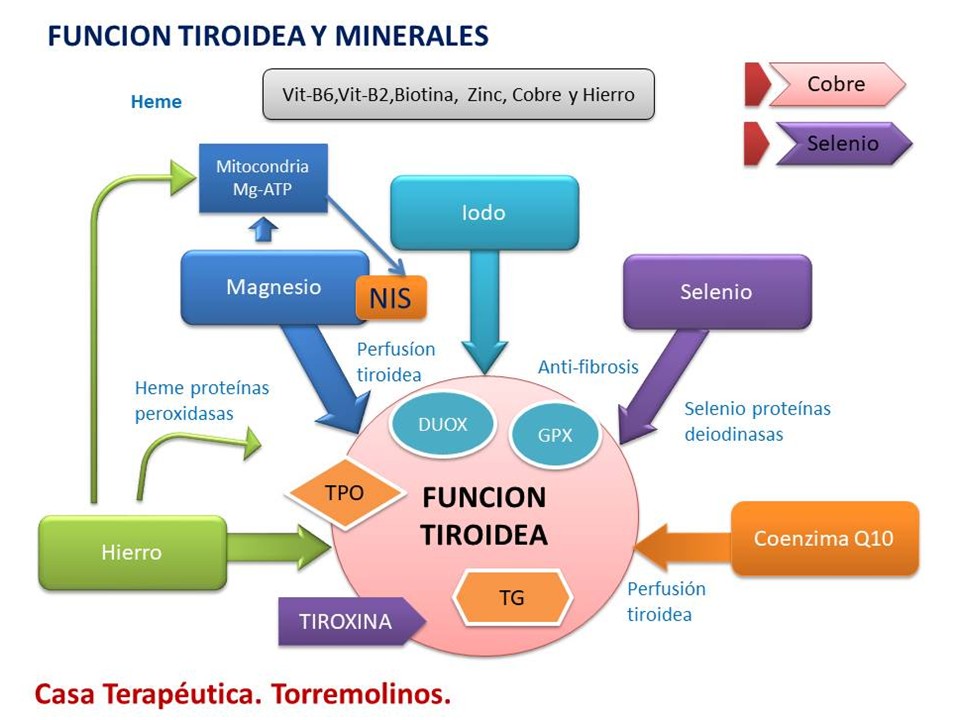
Minerales y Tiroides
Hierro
Los datos experimentales han demostrado que la deficiencia de hierro reduce la actividad de la peroxidasa tiroidea (DOI: 10.1093/jn/132.7.1951). La cinética de las hormonas tiroideas (DOI: 10.1093/jn/128.8.1401 ) también puede verse afectada en la deficiencia de hierro. El papel central que tiene el hierro en la economía de la tiroides se puede explicar por una buena razón: la peroxidasa tiroidea es una hemoproteína. El hemo se produce en las mitocondrias y el camino hacia estos orgánulos requiere una acción coordinada entre la absorción intestinal del hierro, el transporte de hierro y la entrada en el citoplasma y en las mitocondrias ( PMID: 20495089 ). Además del hierro, otros requisitos nutricionales para la síntesis de hemo incluyen: vitamina B6, riboflavina, biotina, cobre y zinc. Además del hemo, las mitocondrias también sintetizan proteínas de hierro-azufre (PMID: 25245479 ) que están relacionadas con la detección de hierro y el suministro de hierro intracelular ( DOI: 10.1016/j.bbamcr.2012.05.009 ). La deficiencia de hierro conduce a la disminución de la expresión de la selenoproteína glutatión peroxidasa (DOI: 10.1093/jn/125.2.293 ) por la cual la función tiroidea puede verse comprometida.
Magnesio
El magnesio desempeña un papel central en el balance de energía, así como también en un proceso descrito como cronometraje celular ( doi: 10.1038/nature17407). Los procesos energéticos diarios del organismo están relacionados con el control circadiano de la biodisponibilidad de NAD (+) (PMCID: PMC3963134). Además del NAD, la regulación del magnesio intracelular parece subyacer a un mecanismo similar (doi: 10.1038/cr.2016.65).
En la publicación original del modelo de enfermedad tiroidal de WOMED, ya se vio la relación del magnesio con los cambios en la perfusión de la tiroides (PMCID: PMC4661500). También la importancia del magnesio en todos los procesos que requieren energía que es suministrada por magnesio-ATP. El magnesio-ATP se produce en el complejo V de la cadena de moléculas de fosforilación oxidativa (OXPHOS) (doi: 10.1007/s10545-011-9382-9 y PMC3788808). Un papel central del magnesio en la economía de la tiroides se puede encontrar en relación con la captación de yodo ( PMC1198477 ). Los datos experimentales han demostrado que altas dosis de magnesio aumentan la actividad de la tiroides (PM:25141541) . La deficiencia de magnesio puede influir en la biodisponibilidad y la distribución tisular del selenio que luego parece disminuir (DOI: 10.1080/07315724.1997.10718669).
Selenio
Consideramos que el lugar principal para el selenio en las funciones corporales está en su propiedad protectora en forma de selenoproteínas (DOI: 10.1210/er.2001-0034). Los principales grupos implicados son la glutatión peroxidasa y las deiodinasas ( DOI: 10.1677/joe.1.05971 ). La tiorredoxina reductasa desempeña un papel importante en la respuesta al exceso de yodo (PMC5417175 ). El daño a la tiroides puede ocurrir en situaciones de exceso de yodo y deficiencia de selenio (DOI: 10.1210/endo.132.4.8462484 ). En condiciones experimentales, una deficiencia combinada de yodo y selenio puede alterar el patrón de distribución tisular de los elementos traza (DOI: 10.1385/BTER:95:3:247 ). . Tanto la estructura, es decir, la pérdida de crestas, como la función de transporte de electrones de las mitocondrias pueden alterarse en la deficiencia de selenio (DOI: 10.1007/BF02784077). Estas acciones sobre la biogénesis mitocondrial se complementan con hormonas tiroideas ( DOI: 10.1111/j.1432-1033.1995.344zz.x ) . Además de la acción conocida de las deiodinasas como selenoproteínas; en el tiroides tiene una influencia positiva del selenio en la expresión de la actividad del simportador de yoduro de sodio (NIS) inducida por TSH ( DOI: 10.1089/ars.2014.6228) . Finalmente, debe destacarse que la síntesis de selenoproteína es también un proceso activo que requiere ATP. En un modelo endocrino se asocia el suministro de energía a través de ATP con magnesio. Además, el selenio intracelular está relacionado con los niveles de magnesio (PMID: 26675817 )
Zinc
La deficiencia de Zn inhibe la síntesis de la hormona liberadora de tirotropina (TRH). Cabe destacar que el hipotiroidismo causa deficiencia de Zn en humanos y, a la inversa, la deficiencia de Zn puede provocar hipotiroidismo [DOI: 10.26717/BJSTR.2018.06.001336]. El zinc también es necesario para el correcto funcionamiento del factor de transcripción tiroideo 2 (TTF-2), que estimula la expresión de los genes de la tiroglobulina y la tiroperoxidasa. Por lo tanto, el zinc es importante en la producción de hormonas tiroideas, ya que la tirotropina y la tiroperoxidasa son proteínas implicadas en la síntesis de T3 y T4 en la tiroides (DOI: 10.1007/s12011-020-02562-5. En condiciones experimentales, un estado combinado de deficiencia de yodo, selenio y Zn puede alterar significativamente la morfología de la glándula tiroides (DOI: 10.1093/jn/129.1.174 )Por lo tanto, el Zn es importante en la producción de hormonas tiroideas, ya que la tirotropina y la tiroperoxidasa son proteínas involucradas en la síntesis de T3 y T4 en la tiroides.. Los bajos niveles de Zn se han descrito por estar relacionados con el desacoplamiento de la actuación de la función mitocondrial en el nivel del citocromo b y c (DOI:10.1016/0006-291x(67)90242-2) que interfieren también con ubiquinona (DOI:10.1016/0014-5793(72)80802-0). El zinc regula la actividad de la deiodinasa hepática y la deficiencia de Zn produce una disminución en la conversión de T4 a T3. (DOI: 10.1080/07315724.1994.10718373).
Cobre
– El cobre es un cofactor de la fenilalanina hidroxilasa, que favorece el paso de fenilalanina a tirosina. También es necesario para la síntesis del hemo. La acción de la hormona tiroidea es mediada por los receptores de hormonas tiroideas TRα1 y TRβ. Los niveles de cobre en suero están regulados por la hormona tiroidea, la cual estimula la síntesis y la exportación hepática de la proteína ceruloplasmina que transporta el cobre en el suero. El receptor TRβ esta relacionado con el cobre y el TRα1 con el selenio ( DOI: 10.1042/BJ20111817 ). Estimulación de la producción de tiroxina (T4) e inhibición de la absorción excesiva de T4 en las células sanguíneas. (DOI: 10.3390/ijms24054840). Además, el Cu es necesario para la síntesis de fosfolípidos, que son esenciales para la estimulación de la TSH [DOI: 10.26717/BJSTR.2018.06.001336 ).
Iodo
El yodo es un sustrato para la biosíntesis de hormonas tiroideas que influyen en el metabolismo y afectan la expresión de genes que controlan diversas funciones fisiológicas, como la embriogénesis, el crecimiento y el desarrollo del organismo . Las concentraciones de TSH, tiroglobulina (TG) y triyodotironina libre (FT3) en suero se consideran indicadores alternativos del estado del yodo [52].Se ha informado que la deficiencia de yodo puede causar un aumento en los niveles de TSH y/o en el volumen tiroideo [PMCID: PMC8223911]. Desafortunadamente, el aumento del consumo de yodo no siempre resulta en una disminución notable de la concentración de TSH, que permanece dentro del rango de referencia. Asimismo, el nivel de tiroxina libre (FT4) cambia muy lentamente después de la administración de yodo [DOI: 10.1007/s12011-019-01943-9]. Kravchenko et al. [DOI: 10.1007/s12011-019-01943-9] sugieren que la TG parece ser un indicador más sensible del estado de yodo después de la reposición. Aumento de la expresión del gen de la proteína de unión a la caja X 1 ( XBP1 ); el XBP1 inhibe la transcripción de genes implicados en la síntesis de TH; por ello el exceso de I inhibe la síntesis de TH. ( DOI: 10.1016/j.mce.2011.09.036).
Manganeso
El manganeso, regula la actividad de la deiodinasa hepática y la deficiencia de Mn produce un aumento en la conversión de T4 a T3 y el exceso produce una disminución de la conversión ( PMCID: PMC2067987)
Cobalto
Altera la captación de yodo por la glándula tiroides e Inhibe la desyodación extratiroidea en posición 5′ de la T4 a T3 y produce aumento de FT4 y disminución de FT3. (DOI: 10.5271/sjweh.1605).
Casaterapéutica. Torremolinos. 29620. Málaga
Tlfno. 646219611. Consulta Médica.

Deja un comentario